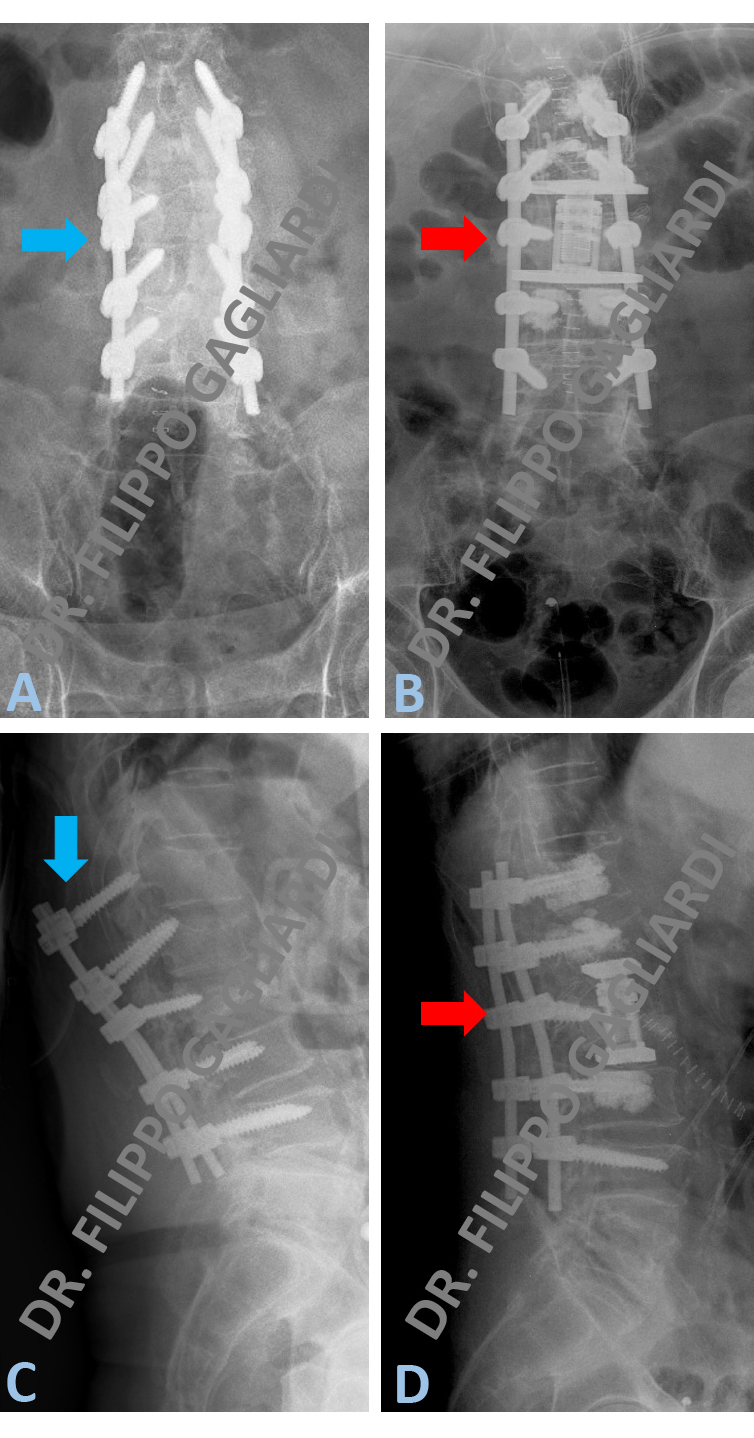
Corpectomia vertebrale lombare Caso di cedimento di un sistema di stabilizzazione vertebrale in seguito ad incidente stradale. Le frecce azzurre nelle Figure A e C dimostrano lo scivolamento posteriore del sistema.
Corpectomia vertebrale lombare
Per ricostituire la stabilità vertebrale il Paziente è stato sottoposto a revisione del sistema con asportazione di un corpo vertebrale rotto (corpectomia). In seguito questo verrà sostituito con una gabbia in titanio (cage) (frecce rosse Figura B e C).
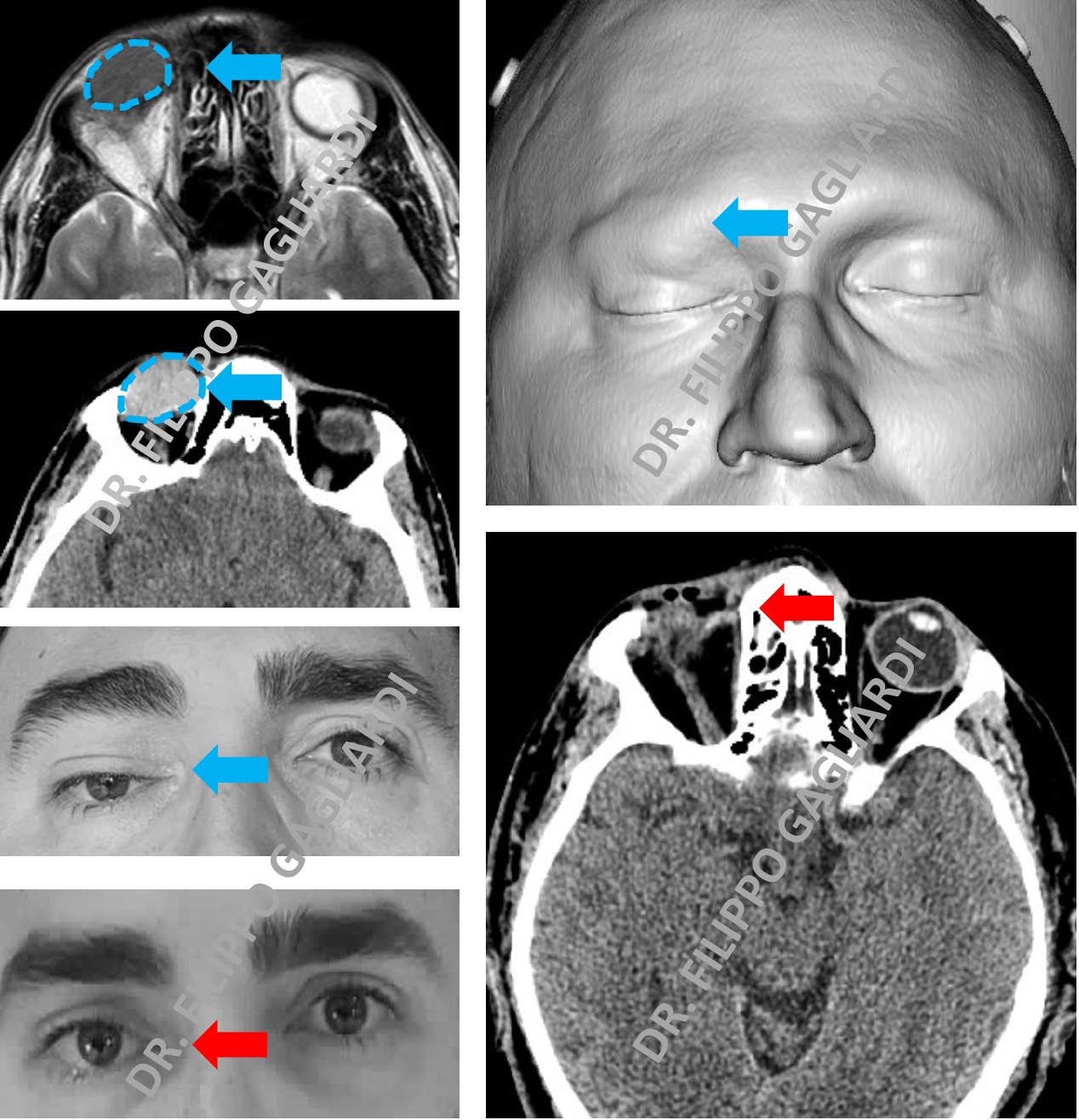
Chirurgia dell'orbita e dei seni paranasali Esempio di chirurgia dell'orbita e dei seni paranasali. Caso di asportazione di una lesione dell’orbita che causava compressione del globo oculare e paralisi della palpebra. Frecce azzurre i reperti prima dell’intervento. Frecce rosse il risultato post-operatorio (immagine gentilmente concessa dal paziente).
Caso di triplice ernia discale cervicale (Figura A) trattata con l’asportazione del disco intervertebrale malato corrispondente ed il posizionamento di 3 gabbiette in titanio munite di piccole viti che le fissano ai corpi vertebrali dando la massima stabilità all’impianto e senza avere necessità di mettere placche di titanio davanti alle vertebre per bloccare le gabbiette. Il controllo post-operatorio (Figura B) mostra il corretto posizionamento del sistema con il ripristino della fisiologica lordosi cervicale.
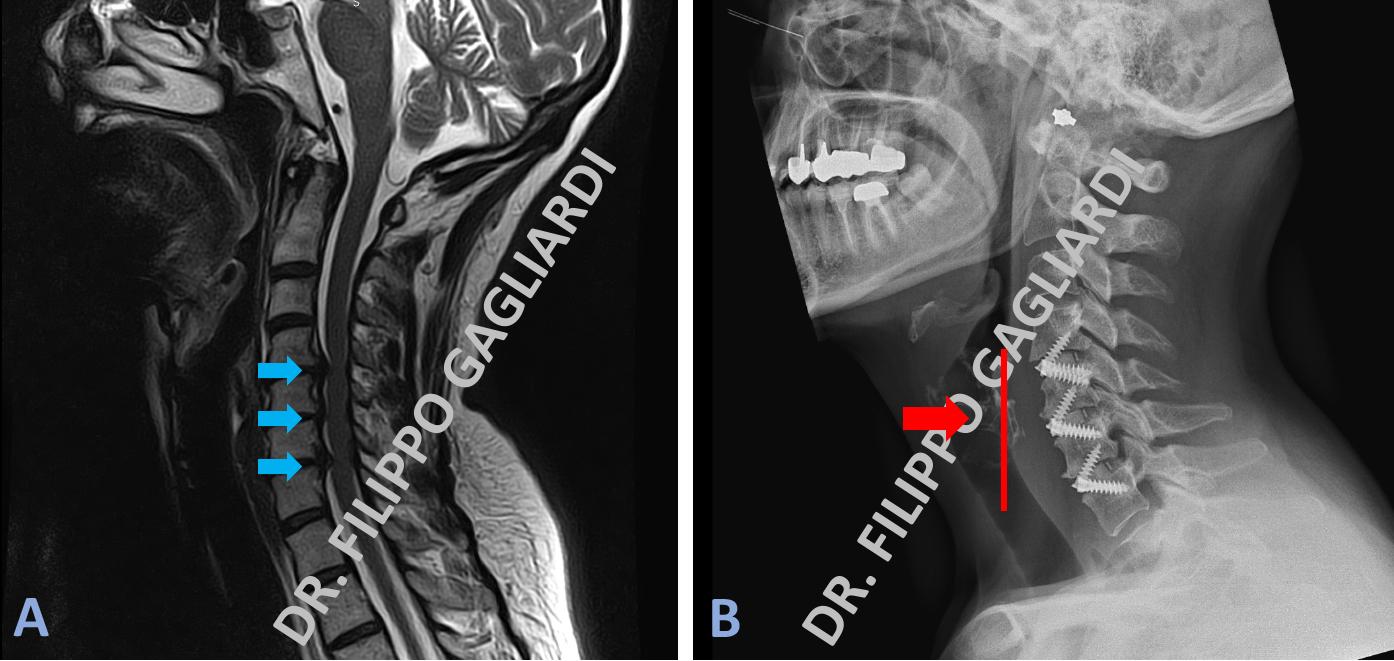
Caso di frattura della quinta vertebra cervicale con scoppio del corpo vertebrale a causa di un incidente della strada. Le frecce azzurre nelle Figure A e C dimostrano lo RX e la TC del collo. Evidente la frattura e la lussazione vertebrale.
Per ricostituire la stabilità vertebrale il Paziente è stato sottoposto ad un intervento in due tempi. La prima fase passando da davanti (tempo anteriore) e poi dietro (tempo posteriore). L'intervento è consistito in una corpectomia (asportazione del corpo vertebrale) della vertebra fratturata. Si è passati, poi, al posizionamento di una protesi espandibile (cage + placca) per via anteriore e viti di stabilizzazione posizionate per via posteriore (frecce rosse Figura B, D, E).
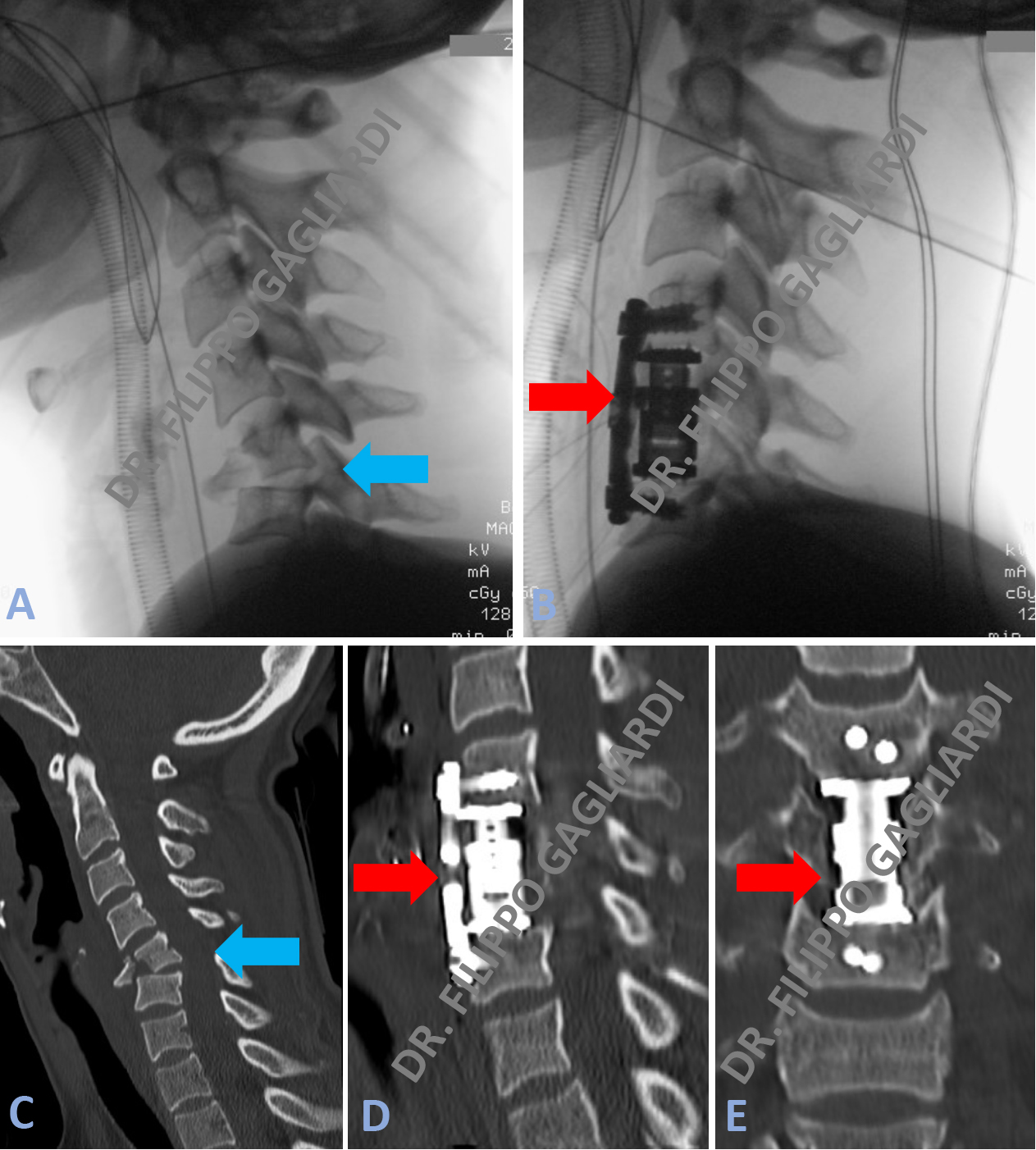 Corpectomia vertebrale cervicale.
Corpectomia vertebrale cervicale.
Anestesia
La craniotomia, ad eccezione della tecnica a paziente sveglio, awake surgery, che ha indicazioni estremamente selezionate, è un intervento che viene eseguito in anestesia generale.
Procedura
La durata è variabile, e dipende per lo più dal tipo di patologia da trattare. Il paziente può essere posizionato supino, prono o in decubito laterale, in relazione al tipo di approccio chirurgico. Il capo viene fissato con una testiera al letto operatorio (e.g., testiera di Mayfield, testiera a ferro di cavallo). Si pratica un’incisione chirurgica estetica dietro l’attaccatura di capelli, rasando i capelli lo stretto necessario. L’incisione è localizzata in corrispondenza della lesione da trattare ed è conformata in base al tipo di accesso chirurgico. Per lo più si utilizzano incisioni lineari.
Craniotomia
Si pratica quindi una apertura nelle ossa del cranio centrata sulla patologia, detta appunto craniotomia. Viene eseguita con il craniotomo, una sega ad alta precisione, e con l’ausilio di microfrese ad alta precisione a punta tagliente o diamantata. L’opercolo osseo viene temporaneamente rimosso e conservato in una soluzione di antibiotico. Estensione e forma della craniotomia dipendono anche in questo caso dalla patologia da trattare. Si espone così la dura madre, l’involucro meningeo che riveste cervello e cervelletto. La si sospende con dei punti di sutura ai margini della finestra craniotomica perchè non si formino raccolte liquide tra dura madre ed osso cranico (sospensione durale). A questo punto di solito si posiziona il microscopio operatorio e si esegue la durotomia, o apertura durale. Inizia quindi la parte centrale dell’intervento. Si identifica la patologia da trattare mediante l’uso, quando indicato, della neuronavigazione, della ecografia intraoperatoria, la realtà virtuale aumentata e la fluorescenza intraoperatoria. Si procede pertanto al trattamento della patologia (e.g.,exeresi di un tumore, evacuazione di una raccolta emorragica, esclusione di una malformazione vascolare, correzione di una malformazione). Terminata la fase centrale, si procede a richiudere la dura madre mediante una microsutura sigillata con colla di fibrina. Può essere necessario utilizzare un patch di materiale eterologo preconfezionato (pericardio bovino) o autologo (tessuti dello stesso paziente, come ad esempio pericranio e galea capitis). Questa tecnica viene detta di plastica durale. Si riposiziona dunque l’opercolo osseo nella sua sede naturale. Lo si fissa con microplacche e viti in titanio, materiale anallergico e RM-compatibile. Se necessario si ricostruisce il pianomuscolare (e.g., muscolo temporale) e si richiude la cute. Si lascia in sede un drenaggio sottocutaneo, che viene rimosso dopo 24 ore. Generalmente si pratica una medicazione compressiva, la classica fasciatura del capo. Per facilitare la guarigione dei tessuti viene mantenuta per qualche giorno.
Decorso post-operatorio
Quando ancora il paziente è addormentato si esegue una TC encefalo di controllo, per documentare gli esiti della chirurgia. Il paziente viene quindi condotto in terapia intensiva per un risveglio lento in un ambiente protetto. Qui vengono monitorizzati tutti i parametri in tempo reale. La mattina successiva viene ricondotto in reparto per la successiva degenza. La craniotomia non è un intervento doloroso poichè il cervello non contiene nel suo contesto terminazioni del dolore. In prima giornata il paziente viene mobilizzato e messo in piedi. Si rimuovono il catetere vescicale e il drenaggio. Vengono ridotti allo stretto necessario gli accessi venosi. La ferita viene medicata con regolarità. Si rimuove la fasciatura compressiva. In terza giornata il paziente può lavarsi i capelli. La successiva degenza ha una durata variabile, mediamente di 4-5 gg.
Convalescenza
La convalescenza a casa, laddove non ci siano problematiche cliniche e neurologiche è di circa un mese. Il paziente conduce una vita normale, astenendosi da sforzi fisici, attività sportiva, possibilmente dalla guida. I farmaci con cui viene dimesso sono di solito l’eparina (somministrazione sottocutanea) che viene mantenuta per i primi 10-15 gg, la profilassi anti-epilettica, quando necessario cortisone a scalare e gastroprotettore. In sede di ferita si lascia un cerotto fino alla rimozione dei punti di sutura, in sintesi dopo 8-10 gg dall’intervento.
Gli angiomi cavernosi, o cavernomi, sono malformazioni vascolari intra-cerebrali, all'interno del tessuto cerebrale. Hanno una ampia diffusione nella popolazione generale e possono essere parte di sindromi genetiche complesse. Per lo più tuttavia sono casi sporadici. Le sedi più frequenti degli angiomi cavernosi sono rappresentate dagli emisferi cerebrali, in particolare: lobi cerebrali, frontale, temporale, parietale, occipitale. Meno frequenti sono i cavernomi cerebellari, dei nuclei della base e del tronco dell'encefalo. Un discorso a parte va dedicato ai cavernomi dell'orbita. Lesioni vascolari dentro la cavità orbitaria; generalmente sono retrobulbari, dietro al bulbo ottico e intraconici, ovvero dentro il cono formato dai muscoli che fanno muovere il bulbo oculare. Anche essi rappresentano un'anomalia di sviluppo del sistema vascolare nel contesto del tessuto nervoso. Permangono pertanto queste strutture venose a basso flusso con associati vasi malformati ed anomalie di drenaggio venoso all'interno del parenchima cerebrale. I cavernomi hanno un basso rischio di sanguinamento, stiamo intorno a 0.5%/5 anni.
Anatomia patologica
Gli angiomi cavernosi sono costituti da ampi spazi venosi (caverne) all'interno dei quali scorre sangue venoso a basso flusso e bassa pressione. Questi spazi sono ricoperti da endotelio (il normale rivestimento dei vasi sanguigni). Al loro interno non è presente tessuto cerebrale, a differenza di quanto avviene nelle MAV. Il rischio di sanguinamento è molto basso. Quando avviene l'emorragia è di solito autolimitante e contestuale alla malformazione. Spesso si repertano segni di micro-sanguinamenti pregressi (orletto emosiderinico). Discorso diverso sono i cavernomi del tronco dell'encefalo (ponte, mesencefalo e bulbo), che hanno un rischio di sanguinamento sensibilmente più alto di quelli cerebrali propriamente detti e che pertanto vanno trattati.
Clinica
I sintomi e segni clinici dipendono dalla localizzazione dell'anomalia vascolare. Nella maggior parte dei casi i cavernomi sono asintomatici e il loro riscontro è incidentale. Caratteristicamente i cavernomi cerebrali si manifestano con sintomi irritativi, crisi epilettiche, parziali o generalizzate, semplici o complesse, e deficit neurologici focali. Il sanguinamento spesso si associa a crisi epilettiche generalizzate (la classica crisi epilettica tonico-clonica) o alla comparsa di un deficit neurologico focale. Gli angiomi cavernosi intra-orbitari possono causare proptosi (sporgenza dell'occhio verso l'esterno), disturbi della motilità oculare e calo del visus. Gli angiomi cavernosi del tronco dell'encefalo possono dare sintomi gravi come deficit dei nervi cranici, come ad esempio deficit della motilità oculare, nevralgia trigeminale, deficit di motilità della muscolatura facciale, deficit uditivi, disequilibrio, disfagia, disfonia, paralisi della lingua, e deficit sensitivi e motori di diversi gradi agli arti.
Diagnosi
- RM cerebrale e Angio-RM. La tecnica diagnostica di elezione del neurochirurgo è la RM encefalo con mezzo di contrasto, con una buona definizione dell’architettura della malformazione.
- Angiografia e Angio-RM. Gli angiomi cavernosi non sono visibili con queste tecniche, non avendo rapporto diretto con la circolazione cerebrale.
Trattamento
Per la loro natura gli angiomi cavernosi vanno trattati quando sintomatici. Il trattamento è chirurgico. L'intervento del neurochirurgo consiste in un intervento di craniotomia ed asportazione della malformazione. Ad oggi la radiochirurgia stereotassica viene utilizzata per il trattamento degli angiomi cavernosi del tronco dell'encefalo, quando questi non siano approcciabili chirurgicamente o per angiomi cavernosi in altre sedi non chirurgicamente accessibili.
Prognosi
La prognosi che il neurochirurgo fa degli angiomi cavernosi è generalmente buona. Buono è il recupero funzionale dei pazienti e il controllo delle crisi epilettiche. Una volta asportati rara è la recidiva. L'intervento chirurgico è considerato curativo. La prognosi degli angiomi cavernosi del tronco è invece più severa, dovuto alla sede critica della lesione. Spesso si associano a deficit neurologici permanenti, spesso invalidanti.
I craniofaringiomi sono tumori epiteliali primitivi del sistema nervoso centrale. Più specificamente i craniofaringiomi sono tumori disembriogenetici che originano da alterazioni nella differenziazione del tessuto nervoso nella fase di sviluppo embrionale. Diverse sono le teorie sul loro sviluppo. In particolare i craniofaringiomi originano da residui di cellule epiteliali del dotto craniofaringeo all'interno del tessuto nervoso. Col tempo queste cellule tendono a crescere generando una massa che comprime le strutture nervose limitrofe e genera un'alterazione funzionale della ghiandola ipofisaria fino all'insufficienza di produzione ormonale. I craniofaringiomi colpiscono prevalentemente la popolazione pediatrica, ma vi è un ulteriore picco di incidenza nell'età adulta, nella quinta decade di età, Il tumore cresce dalla regione della sella turcica (regione sellare) in alto verso l'interno della cavità cranica. Sono state prodotte diverse classificazioni dei craniofaringiomi. Le più utilizzate fanno riferimento alla dimensione e all'estensione anatomica di questi tumori in relazione al loro rapporto con la sella turcica (e.g., lesioni intrasellari, sovrasellari, intraventricolari).
Anatomia patologica
I craniofaringiomi sono lesioni spesso cistiche con componenti solide. Le cisti contengono un liquido torbido definito per caratteristiche morfologiche motor oil (simile all'olio motore delle automobili). Le due istologie più frequenti sono il craniofaringioma adamantinomatoso e il papillare. I tumori adamantinomatosi sono prevalentemente cistici, mentre quelli papillari sono tendenzialmente solidi. I tumori pediatrici sono prevalentemente adamantinomatosi, quelli negli adulti invece sono papillari.
Clinica
Come per gli adenomi ipofisari, i sintomi più comuni sono legati alla presenza della massa tumorale (effetto massa) e alle complicanze ormonali (insufficienza funzionale della ghiandola), la sindrome da deconnessione del peduncolo ipofisario e la sindrome ipotalamica. L'effetto compressivo su chiasmo ottico e nervi ottici porta a deficit progressivo del campo visivo e alla perdita dell’acuità visiva (calo del visus). Il possibile coinvolgimento dell'ipotalamo, la struttura immediatamente soprastante la ghiandola ipofisaria, genera la cosiddetta sindrome ipotalamica. É caratterizzata da alterazioni del comportamento alimentare (obesità ipotalamica), degli elettroliti nel sangue, del ciclo sonno-veglia, del senso della sete (diabete insipido). Il diabete insipido è una condizione che porta il paziente a perdere liquidi attraverso un aumento del volume urinario e a dover introdurre una grande quantità di liquidi per compensare). La sindrome da deconnessione del peduncolo ipofisario è caratterizzata da una insufficienza di produzione ormonale da parte dell'ipofisi associata ad un aumento della produzione di prolattina (in genere inferiore ai livelli di un prolattinoma). Questa situazione genera nella popolazione pediatrica un ritardo nella crescita e dello sviluppo sessuale, che rappresentano i caratteristici sintomi di esordio nel bambino.
Diagnosi
Come per gli adenomi ipofisari, anche per i craniofaringiomi la diagnosi è inizialmente clinica. Necessaria tuttavia è una conferma radiologica, attraverso la RM con mezzo di contrasto. I test ormonali sono utili per valutare il livello degli ormoni ipofisari, così da confermare se vi sia presenza di un eccesso di prolattina, di un deficit di produzione degli altri ormoni e di diabete insipido. Tra gli esami diagnostici indicati vi sono:
- RM encefalo con e senza mezzo di contrasto
- Test ormonali
- Dosaggio degli elettroliti plasmatici e urinari, osmolarità plasmatica e urinaria, volume urinario
- Esami oculistici (campo visivo computerizzato, esame del fundus oculi, test dell'acuità visiva)
Terapia
I craniofaringiomi sono tumori benigni, localmente aggressivi. E' pertanto fondamentale garantire un controllo locale di malattia per curare questo tipo di patologia. L'approccio è multimodale e coinvolge necessariamente chirurgia e radiochirugia/radioterapia.
- Chirurgia. La terapia di elezione dei craniofaringiomi, quando possibile è la terapia chirurgica. In genere l’approccio di scelta per le lesioni a sviluppi sellare è la via transfenoidale. L'approccio transfenoidale un intervento minimamente invasivo, eseguito per via microchirurgica o endoscopica, che permette di rimuovere il tumore riducendo le possibili complicanze e i tempi di degenza. L'accesso chirurgico viene eseguito dal naso, attraverso una piccola incisione nella gengiva al di sotto del labbro superiore. Questa tecnica deve essere eseguita da chirurghi specializzati e necessita di tecnologie dedicate. Tumori di dimensioni maggiori ed estesi a livello sopra-sellare nella cavità cranica possono invece richiedere un intervento di chirurgia transcranica (craniotomia).
- Radiochirurgia. La radiochirurgia è indicata esclusivamente ai casi di recidiva post-chirurgica.
- Stereotassia. Lesioni cistiche possono essere efficacemente drenate con tecniche stereotassiche (drenaggio stereotassico).
- Radioterapia. La radioterapia è indicata nei craniofaringiomi plurirecidivi.
- Terapia medica. La terapia medica consiste nella terapia ormonale sostitutiva e nella soppressione della iperproduzione della prolattina. L'integrazione ormonale nel bambino è fondamentale per consentire uno sviluppo psico-fisico adeguato. La terapia medica a volte richiede l'integrazione anche dell'ormone anti-diuretico (ADH) per il controllo del volume urinario e riequilibrio degli elettroliti plasmatici (cura del diabete insipido).
Prognosi
La prognosi craniofaringiomi è generalmente buona. La chirurgia nella maggior parte dei casi è curativa con la guarigione del paziente. A volte è necessaria una seduta di radiochirurgia adiuvante (post-chirurgica) per controllare eventuali residui post-chirurgici. Come per gli adenomi ipofisari, anche con i craniofaringiomi si preferisce non rimuovere parti di tumore in intimo contatto con strutture vascolari o nervose. Cosí si riducono al minimo il rischio di morbidità operatoria e quindi di deficit neurologici del paziente. Anche in questi casi il controllo lesionale è ottimale. In seguito all'intervento si assiste e ad un miglioramento dei disturbi visivi, quando presenti. Spesso è necessario proseguire permanentemente la terapia sostitutiva ormonale e la terapia per il diabete insipido.
Craniotomia
Anestesia
La craniotomia, ad eccezione della tecnica a paziente sveglio, awake surgery, che ha indicazioni estremamente selezionate, è un intervento che viene eseguito in anestesia generale.
Procedura
La durata dell'intervento di craniotomia è variabile e dipende, per lo più, dal tipo di patologia da trattare. Il paziente può essere posizionato supino, prono o in decubito laterale, in relazione al tipo di approccio chirurgico. Il capo viene fissato con una testiera al letto operatorio (e.g., testiera di Mayfield, testiera a ferro di cavallo). Per la corretta esecuzione di una craniotomia si pratica un’incisione chirurgica estetica dietro l’attaccatura di capelli, rasando i capelli lo stretto necessario. L’incisione è localizzata in corrispondenza della lesione da trattare ed è conformata in base al tipo di accesso chirurgico. Per lo più si utilizzano incisioni lineari. Quindi si procede praticando una apertura nelle ossa del cranio centrata sulla patologia, detta appunto craniotomia. Essa viene eseguita con uno strumento che si chiama craniotomo, una sega ad alta precisione e con l’ausilio di microfrese ad alta precisione a punta tagliente o diamantata. L’opercolo osseo viene temporaneamente rimosso e conservato in una soluzione di antibiotico. Estensione e forma della craniotomia dipendono anche in questo caso dalla patologia da trattare.
Fase Centrale della craniotomia
Cosí facendo si espone la dura madre, l’involucro meningeo che riveste cervello e cervelletto. La si sospende con dei punti di sutura ai margini della finestra craniotomica per evitare la formazione di raccolte liquide tra dura madre ed osso cranico (sospensione durale). A questo punto di solito si posiziona il microscopio operatorio e si esegue la durotomia, o apertura durale. Inizia quindi la parte centrale dell’intervento con l’identificazione della patologia da trattare mediante l’uso, quando indicato, della neuronavigazione, della ecografia intraoperatoria, la realtàvirtualeaumentata,e la fluorescenzaintraoperatoria. Si procede pertanto al trattamento della patologia (e.g.,exeresi di un tumore, evacuazione di una raccolta emorragica, esclusione di una malformazione vascolare, correzione di una malformazione). Terminata la fase centrale, si procede a richiudere la dura madre mediante una microsutura sigillata con colla di fibrina. Può essere necessario utilizzare un patch di materiale eterologo preconfezionato (pericardio bovino) o autologo (tessuti dello stesso paziente, come ad esempio pericranio e galea capitis). Questa tecnica viene detta di plastica durale. Si riposiziona dunque l’opercolo osseo nella sua sede naturale fissandolo con microplacche e viti in titanio, materiale anallergico e RM-compatibile. Se necessario si ricostruisce il pianomuscolare (e.g., muscolo temporale), e si richiude la cute. Si lascia in sede un drenaggio sottocutaneo, che viene rimosso dopo 24 ore. Generalmente si pratica una medicazione compressiva, la classica fasciatura del capo, per facilitare la guarigione dei tessuti, che viene mantenuta per qualche giorno.
Decorso post-operatorio
Quando ancora il paziente è addormentato si esegue una TC encefalo di controllo, per documentare gli esiti della chirurgia. Il paziente viene quindi condotto in terapia intensiva per un risveglio lento in un ambiente protetto dove possano essere monitorizzati tutti i parametri in tempo reale. La mattina successiva alla craniotomia il paziente viene ricondotto in reparto per la successiva degenza. La craniotomia non è un intervento doloroso, il cervello infatti non contiene nel suo contesto terminazioni del dolore. In prima giornata il paziente viene mobilizzato e messo in piedi. Si rimuove il catetere vescicale e il drenaggio e vengono ridotti allo stretto necessario gli accessi venosi. La ferita viene medicata con regolarità. Si rimuove la fasciatura compressiva. In terza giornata il paziente può lavarsi i capelli. La successiva degenza ha una durata variabile, mediamente di 4-5 gg.
Convalescenza
La convalescenza a casa, laddove non ci siano problematiche cliniche e neurologiche è di circa un mese. In questo periodo il paziente conduce una vita normale, astenendosi da sforzi fisici, attività sportiva, possibilmente dalla guida. I farmaci con cui viene dimesso sono di solito l’eparina (somministrazione sottocutanea). Il trattamento si mantiene per i primi 10-15 gg, la profilassi anti-epilettica, quando necessario cortisone a scalare e gastroprotettore. In sede di ferita si lascia un cerotto fino alla rimozione dei punti di sutura, che di solito avviene dopo 8-10 gg dall’intervento.
Idrocefalo trattato con derivazione ventricolo-atriale
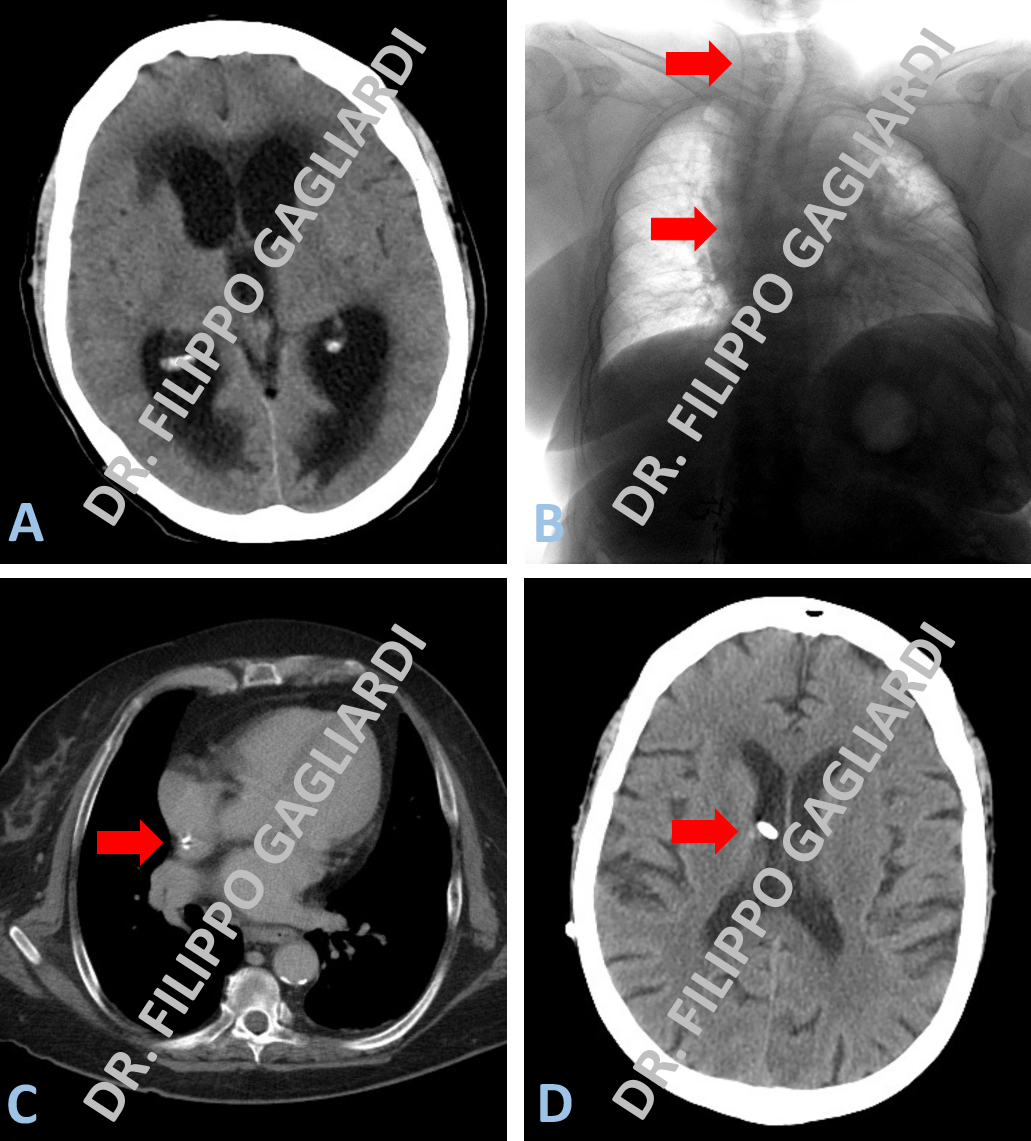
Esempio di derivazione ventricolare in caso di idrocefalo iperteso (dilatazione dei ventricoli cerebrali) condizionante un quadro di ipertensione intra-cranica. I ventricoli, gli spazi neri che si apprezzano all’interno del cranio alla TC pre-operatoria, risultano dilatati. L’alone grigio scuro che li contorna rappresenta la trasudazione del liquido in essi contenuto nel tessuto cerebrale circostante, dovuto all’elevata pressione del sistema (figura A). Il Paziente è stato sottoposto ad un intervento di derivazione ventricolo-atriale, ovvero al posizionamento di uno shunt (drenaggio) che dalle cavità ventricolari, passando nel sottocute della testa e del collo, attraverso la vena giugulare, raggiunge l’atrio destro del cuore dove scarica nel circolo sanguigno l’eccesso di liquido cefalo-rachidiano. La figura B mostra la lastra del torace dove si può apprezzare il decorso del catetere. La figura C mostra l’estremo del catetere, posizionato nel cuore, alla TC torace di controllo post-operatorio; la figura C documenta invece il controllo TC encefalo dopo l’intervento, dove si può notare il ridimensionamento delle cavità ventricolari con la completa risoluzione del quadro di idrocefalo.
Decompressione osteodurale ed evacuazione di ematoma sottodurale acuto
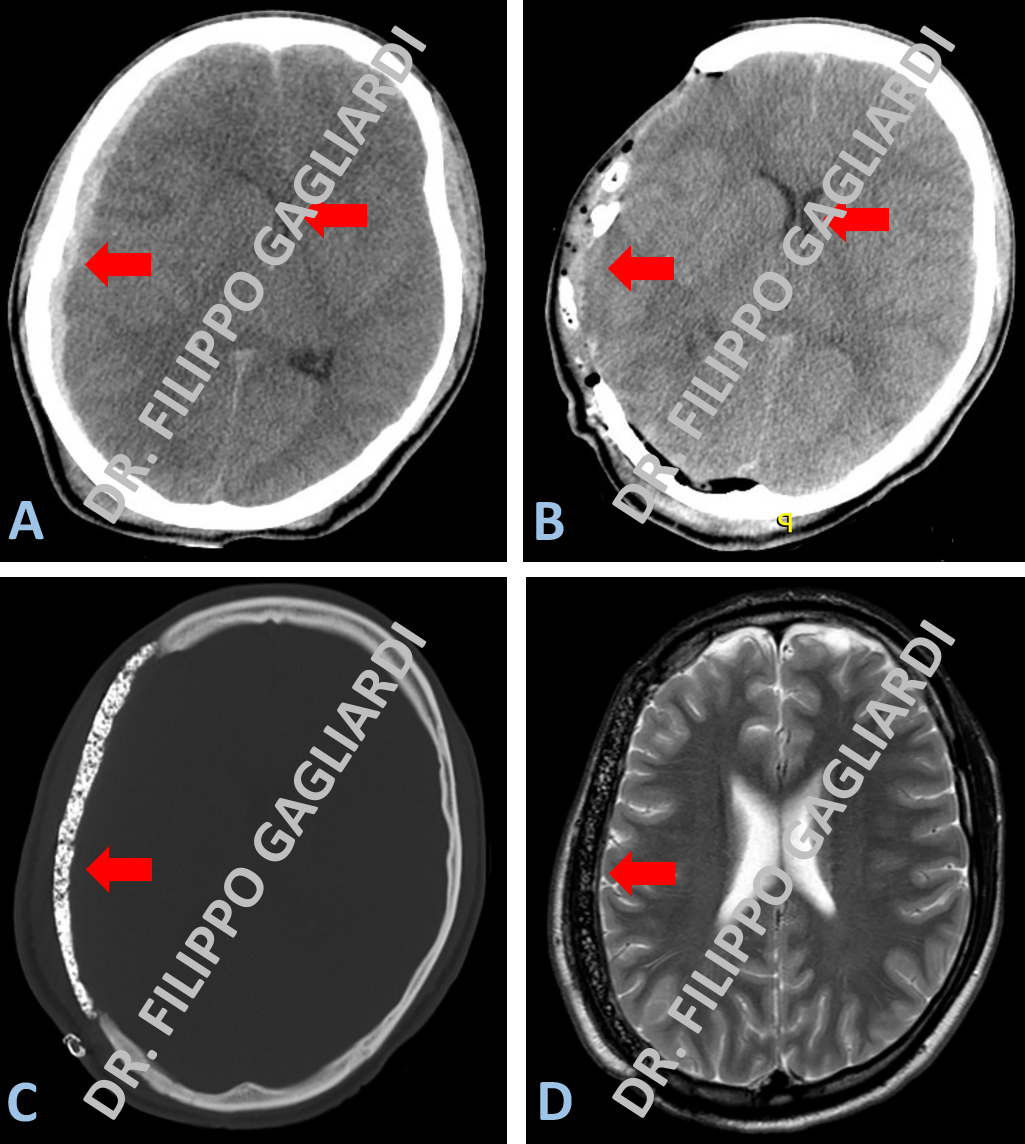
Caso di ematoma sottodurale acuto post-traumatico. L'emorragia sottodurale, immagine iper-densa (bianca) alla TC, presenta la classica forma a semi-luna. L'ematoma si localizza al di sotto della calotta cranica, esternamente all’emisfero cerebrale di destra e condiziona una compressione critica sull'emisfero cerebrale destro, causando una dislocazione del tessuto cerebrale verso il lato opposto (freccia rossa Figura A). La Paziente è stata sottoposta ad intervento di evacuazione dell’ematoma in regime di emergenza e alla rimozione della calotta cranica (decompressione osteodurale) al fine di ridurre la sofferenza da compressione del cervello gonfio in esiti del noto trauma. La TC post-operatoria (Figura B) mostra gli esiti dell’intervento con la evacuazione completa dell’ematoma e la riespansione del tessuto cerebrale (frecce rosse). Le Figure C e D (frecce rosse) mostrano rispettivamente la TC e la RM encefalo a 6 mesi dal primo intervento dopo la ricostruzione del cranio con l’utilizzo di osso sintetico (cranioplastica).
Evacuazione di emorragia intraparenchimale
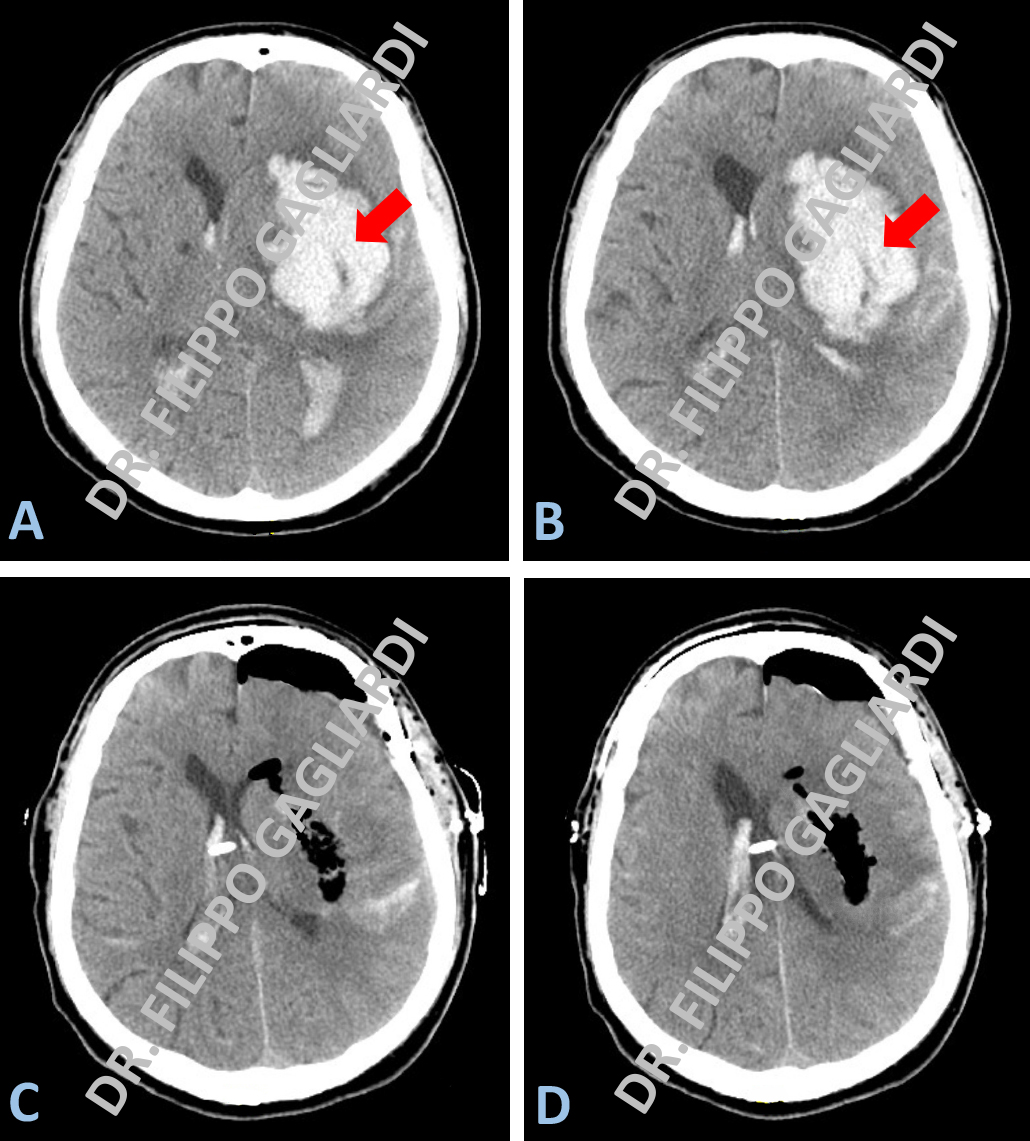
Emorragie cerebrali Tra le emorragie cerebrali, questo è un caso di emorragia spontanea profonda a livello dell’emisfero cerebrale di sinistra. Le Figure A e B mostrano la TC encefalo prima dell’intervento, eseguito in regime di emergenza. Qui si apprezza un’area iper-densa (bianca) corrispondente all’ematoma che esercita un effetto compressivo sulla parte di cervello sano dislocandolo dalla parte opposta. Il paziente è stato operato mediante tecnica mini-invasiva trans-corticale con l’utilizzo di un neuroport (piccolo divaricatore tubulare) con evacuazione completa dell’ematoma. Le Figure C e D mostrano gli esiti dell’evacuazione chirurgica dell'emorragia, con la scomparsa dell’immagine riferibile all’ematoma e la presenza di un catetere di derivazione all’interno delle cavità ventricolari per il monitoraggio della pressione intra-cranica.
Clipping di aneurisma dell'arteria cerebrale media
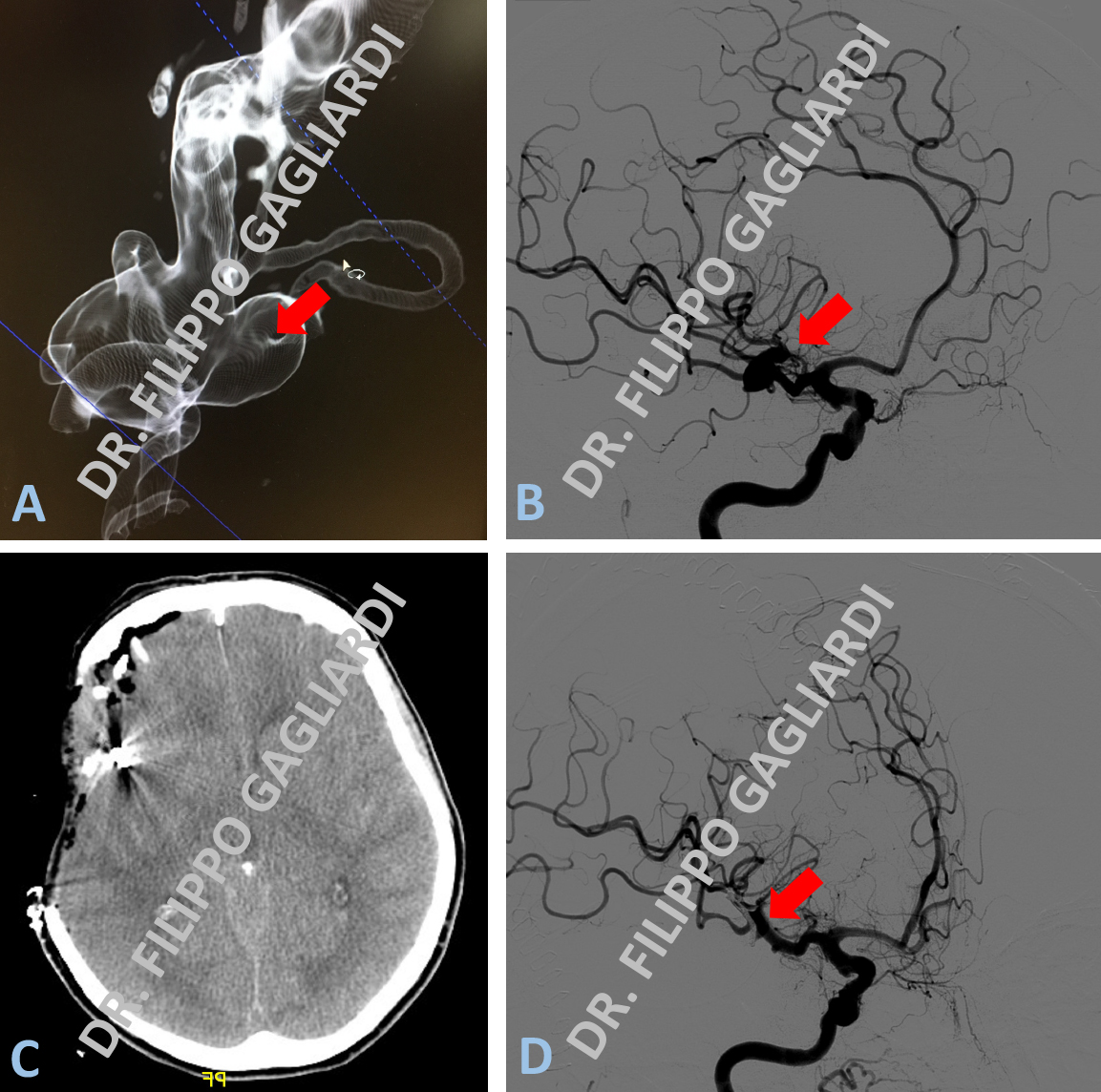
Caso di aneurisma rotto dell’arteria cerebrale media di destra, condizionante un’emorragia cerebrale sub-aracnoidea massiva. Nella Figura A è rappresentata la ricostruzione tridimensionale dell’aneurisma prima dell’intervento chirurgico. La Figura B illustra lo studio angiografico pre-operatorio (la freccia in rosso mostra la dilatazione aneurismatica). Il Paziente è stato sottoposto ad intervento chirurgico in regime di emergenza di craniotomia e clipping (esclusione mediante clip metallica posizionata sul colletto della dilatazione aneurismatica). Visto il quadro di estremo edema cerebrale la teca cranica è stata inviata alla banca dell’osso. Il paziente, quindi, per un periodo è rimasto decompresso (ovvero privo dell’opercolo osseo, successivamente riposizionato una volta risolta la fase acuta). La Figura C corrisponde alla TC post-operatoria. Qui viene mostrata la clip chirurgica in sede e la decompressione del cervello mediante asportazione di parte della calotta cranica. La Figura D mostra l’angiografia cerebrale dopo l’intervento. Si puó notare la completa esclusione dell’aneurisma dal circolo e la preservazione dell’integrità del flusso sanguigno cerebrale.
Clipping di aneurisma dell'arteria comunicante anteriore
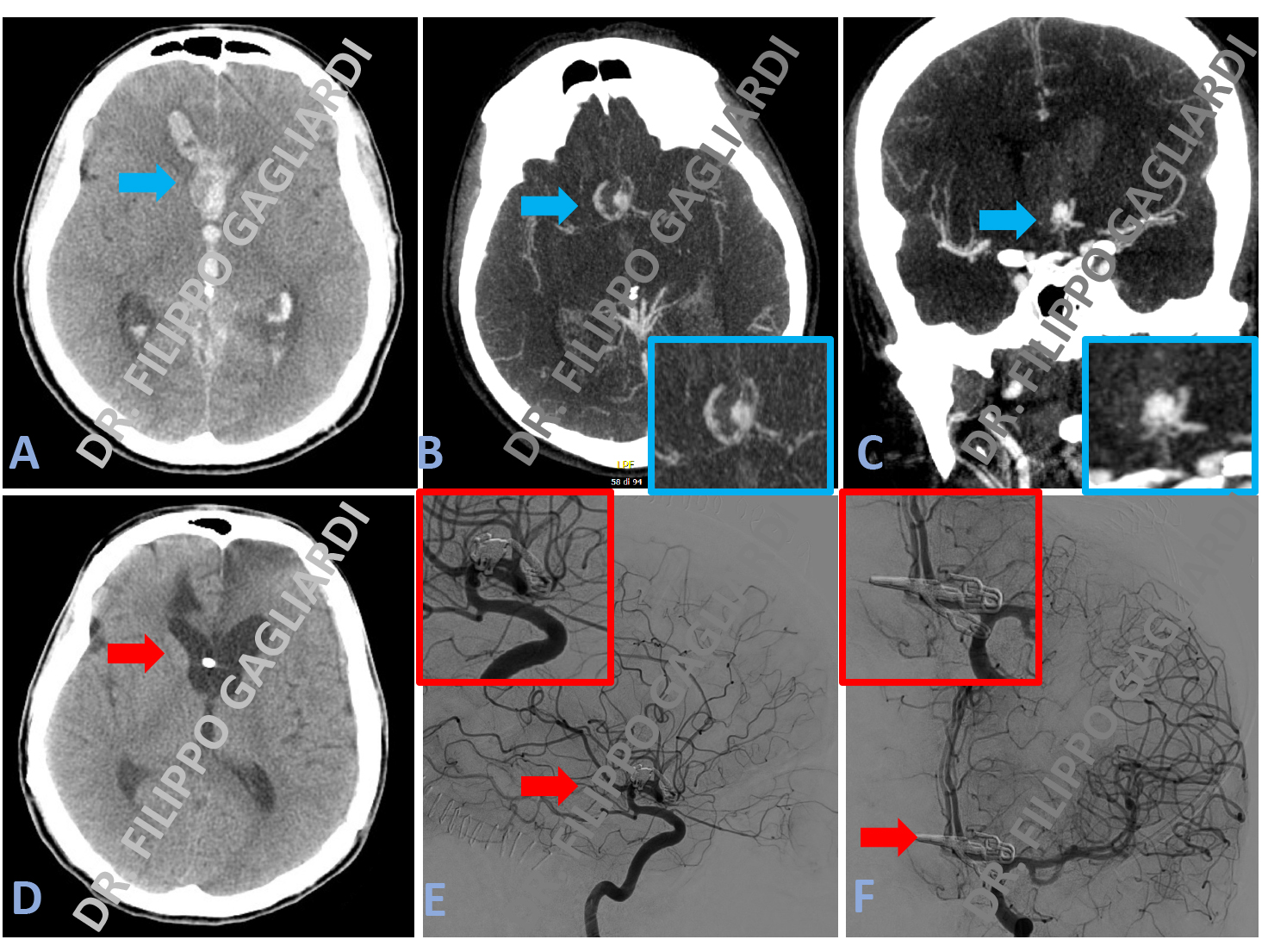 Caso di estesa emorragia cerebrale spontanea (segnale iperdenso/bianco freccia azzurra Figura A) a seguito della rottura di un aneurisma cerebrale a livello dell’arteria comunicante anteriore (immagine tondeggiante, ingrandita nei riquadri azzurri, Figura B e C). Dopo l’intervento l’aneurisma è stato completamente escluso dal circolo mediante l’applicazione di clips. Si é, cosí, arrestata l’emorragia mantenendo integri i vasi sanguigni del circolo cerebrale, come dimostrato dallo studio angiografico (Figura E e F con relativi ingrandimenti nei riquadri rossi). La TC di controllo documenta gli esiti dell’intervento con la preservazione dell’integrità del tessuto cerebrale (Figura D).
Caso di estesa emorragia cerebrale spontanea (segnale iperdenso/bianco freccia azzurra Figura A) a seguito della rottura di un aneurisma cerebrale a livello dell’arteria comunicante anteriore (immagine tondeggiante, ingrandita nei riquadri azzurri, Figura B e C). Dopo l’intervento l’aneurisma è stato completamente escluso dal circolo mediante l’applicazione di clips. Si é, cosí, arrestata l’emorragia mantenendo integri i vasi sanguigni del circolo cerebrale, come dimostrato dallo studio angiografico (Figura E e F con relativi ingrandimenti nei riquadri rossi). La TC di controllo documenta gli esiti dell’intervento con la preservazione dell’integrità del tessuto cerebrale (Figura D).
Dr. Med. Filippo Gagliardi - Neurochirurg Neurochirurgie und Gamma Knife PhD in Molekularmedizin - Neurowissenschaft Krankenhaus San Raffaele - Mailand

Suchen Sie das Ambulatorium in Ihrer Nähe und vereinbaren Sie einen Termin.
Krankenhaus San Raffaele
Via Olgettina, 60; 20132 Mailand (Italien)
Sektor L, Stock -1
Termine unter Tel: 02 2643 2643
E-Mail:
Website: Krankenhaus San Raffaele
Privatklinik Bonvicini
Michael Pacherstr., 12; 39100 Bozen (Italien)
Termine unter: 0471 442700
E-Mail:
Website: Privatklinik Bonvicini
Koala Rehabilitationszentrum
Via abate G. B. Crippa, 19; 24047 Treviglio (BG) (Italien)
Termine unter: 0363 300 337
E-Mail:
Website: Koala Rehabilitationszentrum
 Für Informationen und Kontakte können Sie das untenstehende Formular verwenden.
E-Mail Nachrichten können nur zu informativen, organisatorischen und dringenden Zwecken gesendet werden.
Sie können hingegen nicht als Ersatz einer ambulanten Visite verstanden werden, da die Beurteilung eines klinischen Problems keinesfalls von der Visite und dem Gespräch mit dem Patienten getrennt werden kann.
[contact-form-7 id="1392" title="Contatti_copy"]
Für Informationen und Kontakte können Sie das untenstehende Formular verwenden.
E-Mail Nachrichten können nur zu informativen, organisatorischen und dringenden Zwecken gesendet werden.
Sie können hingegen nicht als Ersatz einer ambulanten Visite verstanden werden, da die Beurteilung eines klinischen Problems keinesfalls von der Visite und dem Gespräch mit dem Patienten getrennt werden kann.
[contact-form-7 id="1392" title="Contatti_copy"]
Operation von Hirntumoren
Zu den Interessensgebieten gehört auch die mikrochirurgische Behandlung von Hirntumoren, Tumoren des Rückenmarks und der Schädelbasis mit fortschrittlichen Neuronavigationstechniken, intraoperativem Ultraschall, kortikaler Stimulation, „awake surgery“/Wachchirurgie, Endoskopie.
Neuronkologische und multimodale Behandlung von Tumoren des zentralen Nervensystems
Neuronkologische und multimodale Behandlung von Tumoren des zentralen Nervensystems, multidisziplinärer Ansatz, kombiniert mit Hirntumorpathologien des Rückenmarks und der Schädelbasis.
Operation der Gefäßerkrankungen des zentralen Nervensystems
Mikrochirurgische Behandlung und klinische Überwachung der Gefäßerkrankungen des zentralen Nervensystems.
Stereotaxie und Radiochirurgie mit Gamma Knife
Behandlung mittels minimalinvasiver radiochirurgischer Technik der Hirntumoren, Gefäßfehlbildungen und Funktionsstörungen.
Rückenchirurgie
Chirurgische Behandlung degenerativer traumatischer tumoröser Wirbelsäulenpathologien.
Hydrozephalus
Operative Behandlung und diagnostischer Klassifikation des Hydrozephalus.
Klinische Forschung über Hirntumoren
Klinische Forschungsprotokolle auf dem Gebiet der molekularen Charakterisierung von Stammzellen aus Hirntumoren, der Aufbau einer Hirntumoren-Biobank und fortschrittliche Bildgebungsprotokolle für Tumore des zentralen Nervensystems.
 Formation.
Formation.
Abschluss mit Auszeichnung in Medizin und Chirurgie an der Universität von Verona (2006). Qualifiziert für den Beruf des Arztes an der Universität von Bologna (2006). In 2013 spezialisierte er sich mit Auszeichnung auf Neurochirurgie bei der Vita-Salute San Raffaele Universität in Mailand. Er legte die Europäische Prüfung in Neurochirurgie am "European Association of Neurosurgical Societies“ (2011) ab. Derzeit ist er als Neurochirurg als Ärztlicher Direktor des Level 1 an der Abteilung für Neurochirurgie des Krankenhaus San Raffaele in Mailand tätig. Er erlangte die wissenschaftliche nationale Qualifikation als Dozent der zweiten Stufe für Neurochirurgie.
Forschung.
Im Rahmen der Forschung erwarb er den Doktortitel in Neurowissenschaften an der “International School of Doctorate“ in Molekularer Medizin an der Vita-Salute-Universität, wissenschaftliches Institut San Raffaele in Mailand. Hier beschäftigt er sich mit Stammzellforschung bei Hirntumoren. Gewinner des internationalen Preises "Karl Storz" (2012). Er war "Research Fellow" an der Klinik für Neurochirurgie der Ludwig-Maximilian-Universität (München, Deutschland) und an der George-Klinik für Neurochirurgie Washington University (Washington DC, USA), mit der er derzeit an zahlreichen Forschungsprojekten und auch regelmäßig an Ausbildungspraktika vor Ort zusammenarbeitet.
Fakultätsmitglied.
Als Mitglied der Fakultät wurde er zu folgenden internationalen Lehrveranstaltungen eingeladen:
-
- 2013 „Der erste jährliche kombinierte Ventrikel- und Schädelbasis-Endoskopiekurs der SLU-Klinik für Neurochirurgie für Neurochirurgen" (Saint Louis, MO, USA).
- 2012 „Third Adelaide Endoscopic Skull Base Course" (Adelaide, SA, Australien).
- 2012 „Internationaler praktischer Sezierkurs“ Vita-Salute-Universität, San Raffaele Scientific Institute“ (Mailand, Italien).
Tutorial-Aktivität.
Er hat auf Einladung praktische tutorielle Lehrtätigkeiten bei folgenden wissenschaftlichen Tagungen und internationalen Kursen der Neurochirurgie abgehalten:
-
- 2014 „Micro Neurosurgical Training Course“ (George Washington University; Washington DC, USA).
- 2012 „Fourth Adelaide Management of Vascular Injuries Workshop“ (Adelaide, SA, Australien).
Didaktische Erfahrungen.
Er hat folgende pädagogische Erfahrungen:
-
- 2013 “"Ausbildung in Neurochirurgie" (Johnson & Johnson Medical Spa, Mailand, Italien).
- 2010-2012 „Tutorial in Neurochirurgie“ (Vita-Salute University, San Raffaele Scientific Institute, Mailand).
- 2002 „Didaktische Tätigkeit in Biologie und Chemie zur Vorbereitung ausländischer Studierender auf Aufnahmeprüfungen an den Fakultäten“ Medizin und Chirurgie", Universität Verona, Italien).
Veröffentlichungen.
Er ist Autor von mehr als 80 wissenschaftlichen Publikationen in internationalen Zeitschriften. Er hat zahlreiche Lehrbuchkapitel über Neurochirurgie geschrieben, die von internationalen Verlagen und Online-Zeitschriften herausgegeben worden sind.
In 2019 veröffentlichte er ein Buch mit dem Titel „Operative cranial neurosurgical anatomy “, das weltweit von einem amerikanischen Verlag veröffentlicht worden ist.
Er hat als "Invited Lecturer" an der Universität Verona (Verona, Italien) Konferenzen und Seminare abgehalten, Macquarie University (Sydney, NSW, Australien) und George Washington University (Washington DC, USA).
Klinische Interessengebiete.
-
- Kraniale und spinale Neuroonkologie.
- Gefäßpathologie.
- Hydrozephalus und kraniale und spinale Fehlbildungspathologie.
-
Degenerative und traumatische Pathologie der Wirbelsäule.
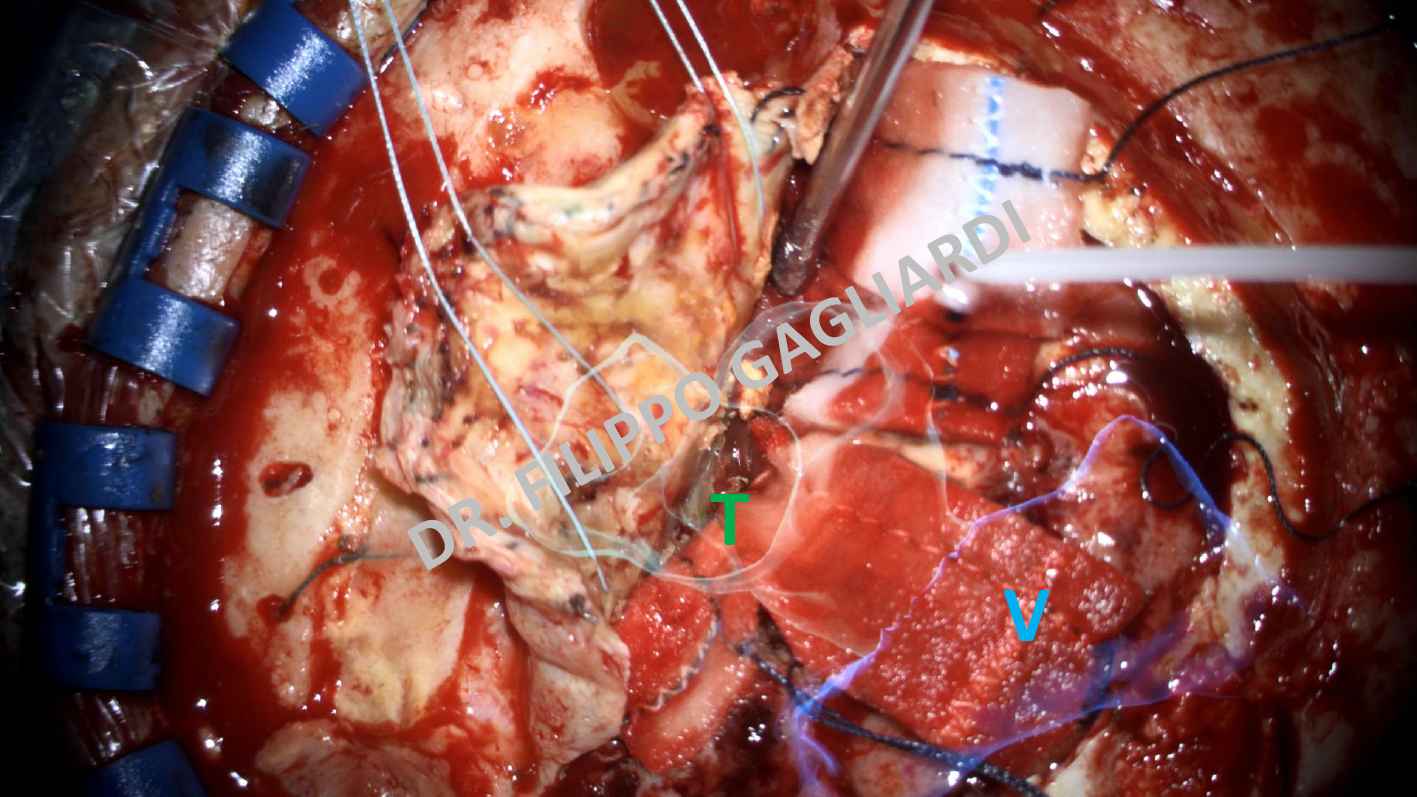
Realtà virtuale aumentata
La realtà virtuale aumentata è una tecnologia che consente letteralmente di “iniettare” nella visione al microscopio del chirurgo immagini acquisite da sistemi di imaging pre-operatorio (RM). Le immagini di risonanza acquisite pre-operatoriamente vengono ricostruite da software di ultima generazione nelle 3 dimensioni selezionando le strutture di interesse (ROIs ovvero Regions Of Interest). Queste immagini ricostruite vengono superimposte alle immagini visualizzate nel microscopio operatorio in tempo reale durante la chirurgia. Cosí si definisce l’esatta posizione della malattia rispetto alle strutture anatomiche critiche attorno ad essa, che devono essere risparmiate. Si forma cosi una fusione di immagini reali e ricostruite superimposte. Il chirurgo potrá aumentare la precisione dell’orientamento e della tecnica chirurgica. Pochi centri al mondo, il San Raffaele è uno di questi, dispongono di questa tecnologia all’avanguardia. In questa immagine, tratta da una delle procedure chirurgiche del Dr. Gagliardi si apprezza la visione, al microscopio operatorio, campo chirurgico. In trasparenza si vede il tumore (volume in verde) e il ventricolo cerebrale (volume in blu). L’integrazione di questa tecnologia con la neuronavigazione consente al sistema di adattare in ogni istante la posizione delle ricostruzioni digitali con l’anatomia reale, correggendo eventuali errori di posizione.